丝素蛋白纳米纤维水凝胶——慢性伤口感染新型敷料
来源:医用蚕丝科技 | 作者:丝素研究院 | 发布日期: 2024-08-07 | 阅读次数:1103次
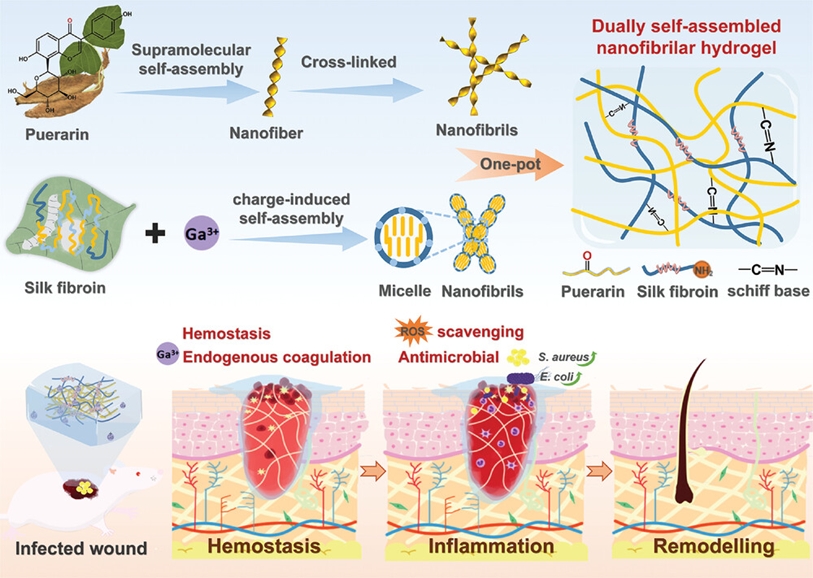
伤口愈合是一个复杂而动态的过程。当伤口表面的细菌群落被自产的细胞外聚合物进一步包裹时,就会形成一个新的生态系统,即生物膜。生物膜成熟引起的细菌毒力和致病性增强,是造成伤口愈合困难的重要因素。镓 (Ga) 是一种通常用作临床诊断和化疗剂的 IIIA 族金属,Ga离子可以运输到细菌细胞中,最终导致细菌死亡。山东大学陈静研究员等提出了一种用于治疗感染伤口的超分子水凝胶敷料,该敷料由小分子葛根素和生物大分子丝素蛋白的双重自组装产生,并通过希夫碱键合将Ga离子掺入水凝胶基质中,使水凝胶具有优异的止血和抗菌性能。
研究内容
将含有Ga离子、SF和葛根素的浑浊溶液加热并搅拌至完全溶解。冷却后形成白色不透明水凝胶。葛根素、葛根素-SF和葛根素-SF-Ga水凝胶分别命名为Px、PxFy和PxFyGaz,其中x、y和z分别是葛根素、SF和Ga离子的浓度。TEM成像中观察到具有纳米纤维状网络结构的葛根素-SF-Ga水凝胶。FTIR和XRD证实了SF与葛根素在凝胶化过程中的相互作用以及二级结构的转变。Ga离子在促进SF无规卷曲向β片构象转化方面具有促进作用。

图1 水凝胶的制造和表征
利用透射电镜(TEM)拍摄了水凝胶的微观形貌,揭示了双纳米纤维共组装形成水凝胶的动态过程。加热的P1F1溶液滴在支撑膜上后,SF在葛根素纳米纤维的外围仍以球形结构存在,但其体积比单独使用SF的体积大得多,表明发生了聚集。然而,当Ga离子和SF一起加热时,圆形胶束发生变形,梭形SF小分子重新排列形成棒状结构,进一步组装形成纳米纤维。加热后,P1F1Ga0.05的SF和葛根素之间形成了交织的双纳米纤维结构。

图2 电荷诱导SF纳米纤维的形成机理
使用旋转流变法验证了双纳米纤维水凝胶的力学性能和热稳定性。0.01–1%应变范围是水凝胶的线性粘弹性区域。添加Ga离子后,水凝胶的屈服应变点为7.05%。Ga离子可以诱导交联密度的增加,从而大大提高了水凝胶的机械强度。随着应变值的变化,水凝胶在凝胶态和溶胶态之间呈现交替过渡,当凝胶状态恢复时,G′和G“与开始时相同,表明水凝胶具有自愈能力。水凝胶的黏度随着剪切速率的增加而降低,表明水凝胶存在剪切稀化性能和可注射潜力。

图3 水凝胶的流变学表征
研究了葛根素在体外不同时间从超分子水凝胶中累积释放。Ga诱导SF发生构象变化,与葛根素纳米纤维交织形成更稳定的双网状结构,从而增加了延长释放时间,P3F1Ga0.1在26 h时释放率达到50%。3种凝胶在72 h的最终释放率均超过95%,证明了药物自组装水凝胶基质具有高负载量和高释放量的优势。
P3F1的溶血率相当低,表明水凝胶中的SF改善了葛根素的溶血,使其可以安全地用于伤口治疗。随着Ga阳离子的添加,溶血率略有增加,但仍保持在<5%,处于生物材料溶血的临界安全范围内。葛根素和SF均具有优异的生物相容性,共培养后细胞活力与对照组无显著差异。
有效的抗氧化剂可以维持细胞内氧化还原平衡,这对感染伤口的修复具有重要意义。所有含葛根素的水凝胶均表现出优异的自由基清除活性和ROS清除能力,表明水凝胶优异的抗氧化性能可用作理想的抗菌敷料。

图4 水凝胶的体外释放、生物相容性和抗氧化效率
Ga独特的Fe模拟特性使其能够通过竞争与细菌细胞内的Fe载体结合来抑制细菌维持生命的活动,从而导致细菌死亡。Ga离子对大肠杆菌的杀菌能力略高于金黄色葡萄球菌的杀菌能力。当Ga离子浓度超过0.025%时,水凝胶对两种细菌的杀菌率均接近100%,实现了接近100%的抗生物膜效果。当Ga离子浓度为>0.05%时,P3F1Ga水凝胶表现出与庆大霉素(阳性对照)相似的显著杀菌率和抗生物膜活性,表明其作为一种新型抗菌敷料可以作为促进感染伤口愈合的新型抗生素替代品。

图5 水凝胶对金黄色葡萄球菌和大肠杆菌的体外抗菌活性
使用小鼠肝出血模型来模拟伤口急性出血的过程。将未治疗的小鼠和接受商业止血敷料治疗的小鼠分别设置为空白对照组和阳性对照组。与空白组的失血量为113.3 mg相比,P3F1Ga0.05水凝胶表现出快速止血,总失血量仅为13.3 mg。P3F1也表现出一些促止血特性,并具有与阳性对照组相似的止血作用,这可能归因于水凝胶本身的物理屏障效应。P3F1Ga0.05中的Ga离子通过激活体内内源性凝血途径来实现止血。因此,超分子纳米纤维水凝胶在物理屏障和Ga离子的双重作用下实现了伤口的快速止血,这对于伤口愈合的第一阶段具有重要意义。

图6 水凝胶的止血性能
选择P3F1Ga0.05来评价水凝胶体内对小鼠全层金黄色葡萄球菌感染伤口模型的治疗效果。建立小鼠感染模型,分别用Tegaderm(空白对照),P3,P3F1,P3F1Ga0.05和Aquacel Ag(商业敷料)治疗。处理10 天后,P3F1Ga0.05处理的小鼠伤口完全闭合,Tegaderm组、P3组、P3F1组和Aquacel Ag组的闭合率分别为71.4%、83.2%、90%和95.7%;P3F1Ga0.05 和 Aquacel Ag 组伤口中的细菌菌落明显较少,这表明P3F1Ga0.05水凝胶在伤口修复方面比市售的含Ag抗菌敷料更好。P3F1Ga0.05组中发现最小的疤痕面积,表明其在应用于伤口时在恢复皮肤原始功能和形态方面的重要性。
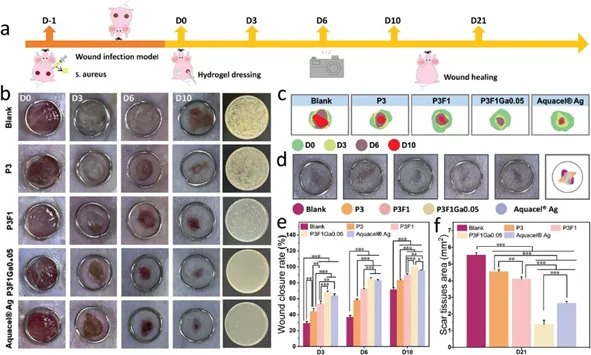
图7 P3F1Ga0.05 水凝胶可加速金黄色葡萄球菌感染的伤口愈合
第3天在P3F1组中观察到明显的新表皮延伸,这主要归因于SF对细胞的增殖和募集作用。肉芽组织的形成是随后组织重塑和愈合的基础,这促进了伤口的快速修复。第6天各组伤口区域均形成肉芽组织,且P3F1Ga0.05组的肉芽组织最厚、最致密。在伤口愈合的后期阶段, P3F1Ga0.05组的再上皮化程度最大,表皮厚度最低,最接近正常组织。

图8 组织学评估水凝胶对感染伤口的治疗效果
在第 10 天分别对每组进行促炎标志物 TNF-α 和抗炎标志物 IL-4 的免疫荧光染色。空白对照组TNF-α因子(红色)的高表达表明,由严重细菌感染引起的伤口炎症持续时间延长,使伤口愈合困难。P3F1Ga0.05水凝胶组表现出最低的TNF-α表达率。IL-4绿色荧光在P3F1Ga0.1水凝胶组中的高表达表明,伤口在第10天已经退出炎症期并进入增殖期,证明了P3F1Ga0.1水凝胶在促进感染伤口愈合方面具有出色的治疗和免疫调节活性。

图9 水凝胶的抗炎特性
结论
成功制备了一种具有双纳米原纤维结构的超分子水凝胶抗菌敷料,用于治疗慢性感染伤口。带正电荷的抗菌Ga离子诱导SF胶束重排,SF与葛根素组装形成双纳米纤维结构,有效增强了所得超分子水凝胶的机械强度和热稳定性。葛根素的天然抗氧化特性可缓解由过量ROS引起的氧化应激,并促进感染伤口从炎症期向增殖期的过渡。此外,SF赋予水凝胶优异的生物相容性,并改善了单独使用葛根素引起的溶血反应。制备的水凝胶具有高效的抗菌和伤口修复性能。因此,这种双纳米纤维超分子水凝胶作为一种新型抗感染敷料具有很强的竞争力,为感染伤口的治疗提供了一种新的策略。
通讯作者简介
陈静,山东大学研究员,博士生导师。组建组织器官修复与再生生物材料课题组,主要研究方向为含糖水凝胶在骨科创面、骨软骨缺损、脊柱脊髓损伤等临床疾病治疗领域的应用。主持国家自然科学基金等产学研项目20余项,在Chem. Soc. Rev等重要学术期刊上发表论文61篇。
原文链接:
https://doi.org/10.1002/adhm.202400071
(esilk.net声明:本网登载此文旨在传递更多行业资讯,文章内容仅供参考。)
